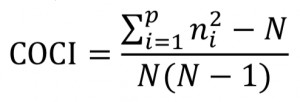研究背景介紹
照護持續性的概念包含了兩個要素:醫療照護服務的整合以及這些服務如何隨著時間改變。1 近年來,提高患者的照護持續性是病人照護的中心主題之一。 較高的照護持續性與好的病人預後相關,包含:急診就診次數減少,入院次數減少和醫療費用降低等,同時也發現,這個效果可以通過減少不適當的藥物得到部分解釋。2 除此之外,較高的照護持續性也可以增加患者的藥物依從性。3 不良的照護持續性會增加發生藥物相互作用事件的風險,並且在多共病的病患中效果更顯著。4 然而,過去鮮少有研究深入探討高照護持續性對於藥物相互作用的影響機制。了解照護持續性如何影響藥物相互作用事件發生的機制非常重要,其原因有二:首先,忽略中介效應可能會導致估計的偏差進而使研究結果無效。其次,中介效應分析可檢視通過控制中介因子後,照護持續性對藥物交互作用的效果,並針對作用機制改善政策介入方向。但目前照護持續性文獻中很少涉及照護持續性的機制。
藥物交互作用是老年病患的常見現象。過去研究發現,嚴重潛在藥物交互作用在全國盛行率為9.3%,而在老年族群的盛行率更高。5 但是,藥物交互作用相關的不良反應通常是可以預測和修正的。6 在老年人群中,有研究發現許多因藥 物相關毒性的住院,其原因是來自於可預期的藥物交互作用。7 多重用藥一詞用以描述同時使用多種藥物的狀況,且被證實為藥物交互作用的風險因子。5,6 即便所有藥物皆遵循治療指引開立,仍可能產生藥物交互作用。8 隨著共病症的盛行以及更多醫生參與治療,多重用藥成為了必然的結果。老年人中共病症的盛行率高,使得多重用藥成為該人群的普遍現象。8 門診病人中,39.4%的老年人口為多重用藥,其中 35%以上的人為持續性多重用藥狀態。9 多重用藥問題的處理 一直是老年患者照護的重要議題。
增加照護連續性可做為減少藥物數量的策略。一回顧性研究發現照護持續性 對藥物產生保護作用,而對於患有多種合併症的老年患者保護效果更大。10 日本的一項研究發現,沒有固定醫生的老年患者發生多重用藥的可能性是有固定醫生的患者的 2.5 倍。11
本研究的目的是建立照護持續性與藥物交互作用之間的關係,並探討多重用藥是否是此項關係的中介因子,並檢測中介作用的程度。
研究方法
此研究使用台灣全民健康保險(NHI)資料庫。全民健康保險計劃自1995年開始在台灣實施,為一強制性保險。迄今為止,國民納保率已達到99.9%。資料庫中包括在住院和門診所進行的各種醫療項目、處方資料及相關的醫療記錄。研究期間為 2011-2017年。全民健康保險資料經常被用於藥物和藥品的研究,因為它可以提供調查研究中無法確定的關於藥物處方的準確資訊。12
老年人口定義為 65 歲及以上的人並蒐集其所有門診就診率及處方資料,篩選符合以下納入標準的患者:(1)該患者自2011年以來必須存活超過 1 年;此納入標準的原因為照護持續性指數(COCI)只能在一個時期內而不是在特定時 間點進行計算,並且(2)在研究期間,患者每年必須有3次以上就診紀錄。因只有在合理的就診次數下才能計算出照護持續性指數(COCI)。使用這些納入標準,2011年共納入 2,318,766 人。
我們使用照護持續性指數(COCI)來衡量照護連續性。過去研究指出,這種計算方式更適合門診就診次數較高的醫療體系。13 照護持續性指數(COCI)為測量一段時間內的就診集中度。14 計算公式如下15 :
ni 特定醫生 i 的看診次數
p 為診治此患者的醫生總數
N 為就診總次數
過去的研究中使用了各種藥物數目切點來定義多重用藥。16 但是,大多數研究使用五種藥物作為定義之切點 9,17-19,因此我們在研究中也採用了該臨界值以確保研究的可比性。在三個月內同時使用五種以上藥物的患者被視為多重用藥,而同時使用超過十種藥物的人則被定義為嚴重多重用藥。12,20
本研究藥物的部分,僅探討西藥部分,而排除了中草藥和非處方藥物,另外,也將局部用藥排除。藥物辨識方面,我們應用了藥物治療分類代碼(ATC)系統作為分類指標。
在藥物交互作用研究中有許多種定義的方式,例如使用知識庫(KB)6,21 以及使用單一國家或地區的臨床評估系統。22,23 但並非所有的藥物交互作用都有足夠的臨床重要性,為了說明藥物交互作用的臨床嚴重性,則需加入專業人員來進行評估。24,25
本研究使用了 Phansalkar 等人提出的藥物交互作用列表,這些藥物交互作用經由專家會議確認為具有臨床意義。26 而該列表也被應用於研究及實際臨床運用。 4,27,28 我們之所以選擇此列表所列之藥物交互作用作為我們的對象是因為:(1) 其所列藥物交互作用組合經由常用之不同的知識庫進行了交叉比較;(2)該列表由具有不同背景的專家小組嚴格審查,並一致認為在臨床決策中應列為警示 (3) 列表以藥物學名或是機轉類別呈現,使我們可以與資料庫建立良好對照。為符合研究需要,本研究對列表做了一些調整,排除了 2 種未被健保給付之藥物組合。藥物交互作用事件被定義為兩種目標藥物,處方期間至少重疊一天。在我們納入 研究的 13 種藥物交互作用組合中,有 4 種組合未出現在結果之中。最後的分析中,僅包含 9 種藥物交互作用組合。
因為各因子為同時測量的,我們採用了反事實因果模型(counterfactual method),驗證多重用藥在照護持續性和藥物交互作用之間起中介作用的假設。29 傳統上中介作用分析方法有兩種,即乘積法和差異法。差異法是將暴露因子對結果的原始影響與針對中介因子效果的結果相減。而乘積法通過將暴露因子對結果的影響與中介因子對結果的影響相乘來估算中介作用。就統計學而言,乘積法可能會受到樣本量的影響,而差異法則趨於保守且低估了中介效果。30 傳統方法因缺乏因果關係的解釋,導致對間接效應的估計有偏差,且在非稀有結果中使用邏輯式回歸或具有因子間的交互作用時,會造成對中介效果的結論不正確。31,32
我們使用了 VanderWeele 提出的四向分解 (four-way decomposition) 33 檢視 3 暴露因子對結果的總體影響。四向分解是一種將整體效果分解為四個部分的方法:直接效果(CDE),參照交互作用(INTref),中介影響之交互作用(INTmed)和單純間 接效果(PIE)。估計過程中需要兩個邏輯式回歸模型:其一為針對結果,另外則為針對中介因子所作的估計。34 我們根據照護持續性指數的中位數定義了高照護持 續性組和低照護持續性組。藥物交互作用和多重用藥狀態皆為二分變項(有無藥物交互作用或多重用藥)。
在敏感性測試(sensitivity analysis)的部分,我們分別重新定義了照護持續性, 多重用藥狀態和藥物交互作用,以測試我們的研究結果可信度。照護持續性改為 使用兩次就診來重新計算照護持續性指數。35在定義多重用藥和嚴重多重用藥時,我們使用了較長的時間範圍。假設患者反覆且持續接受5種以上藥物超過181天,則被定義為持續性多重用藥。36 而此時間區段也被用於定義持續性嚴重多重用藥。20 藥物交互作用則重新定義為目標藥物合併使用超過兩天,以確保我們的結果 對這一更嚴格的定義仍為有效。另外,我們還通過使用三分位數將研究對象重新分組為低,中和高照護持續性組。2,37
子族群分析中(結果未顯示),我們選擇已被證明會對照護持續性和多重用藥產生影響的兩個人口統計學特徵。在韓國進行的一項針對 65 歲以上糖尿病,高血壓,哮喘和慢性阻塞性肺病患者的回顧性研究發現,男性的照護持續性高於女性,並且隨著年齡的增長而降低。37 另外,男女在藥物治療態度和就醫行為方 面也存在顯著差異。研究表明,女性的就醫率比男性高,並且對藥物療法持更積極的態度,而老年人更有可能使用多種藥物。38,39
所有統計分析皆使用 STATA MP Environment (StataCorp. 2017. Stata Statistical Software: Release 15. College Station, TX: StataCorp LLC.).
研究結果
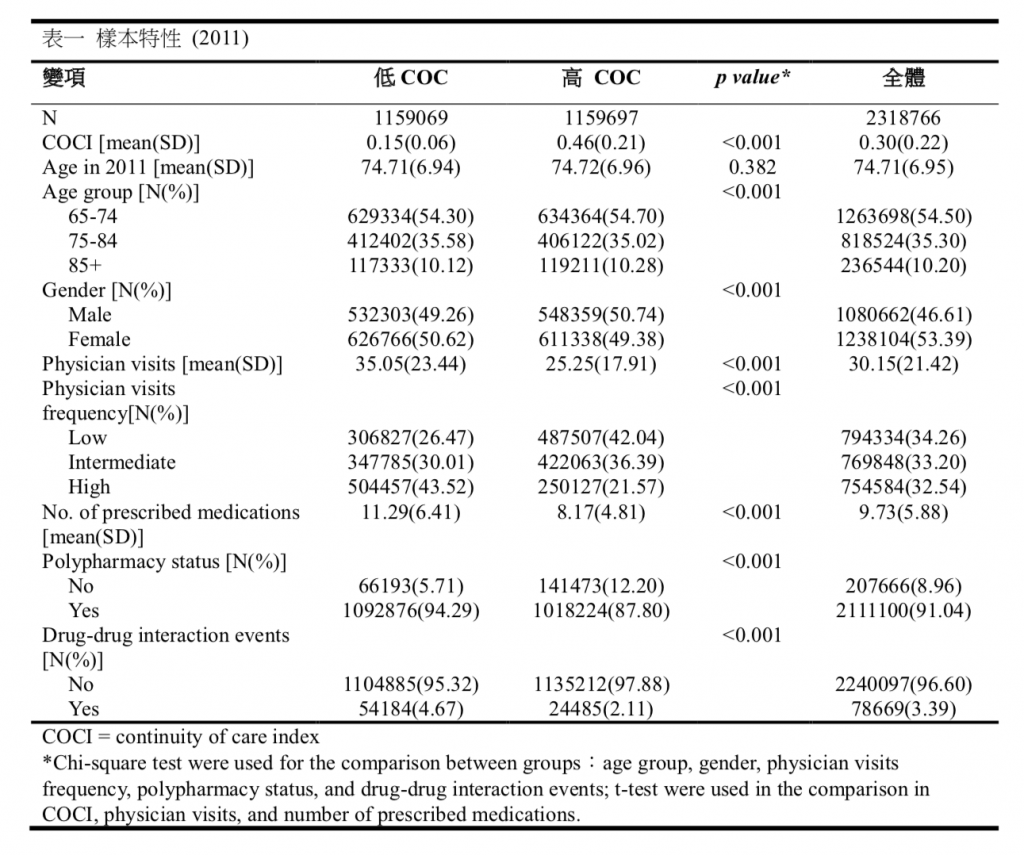
表 1 顯示了研究人群的基本特性,依照護持續性高低分組呈現。兩組之間的性別和年齡存在顯著差異(p <0.001)。高照護持續性組的就診次數,處方藥數量以及發生多重用藥和藥物交互作用事件的患者比例顯著低於低照護持續性組(p <0.001)。 在研究期間,照護持續性指數的平均值略有波動。亦觀察到多重用藥和嚴重多重用藥的比例略有增加,而藥物交互作用的比例也有所增加。
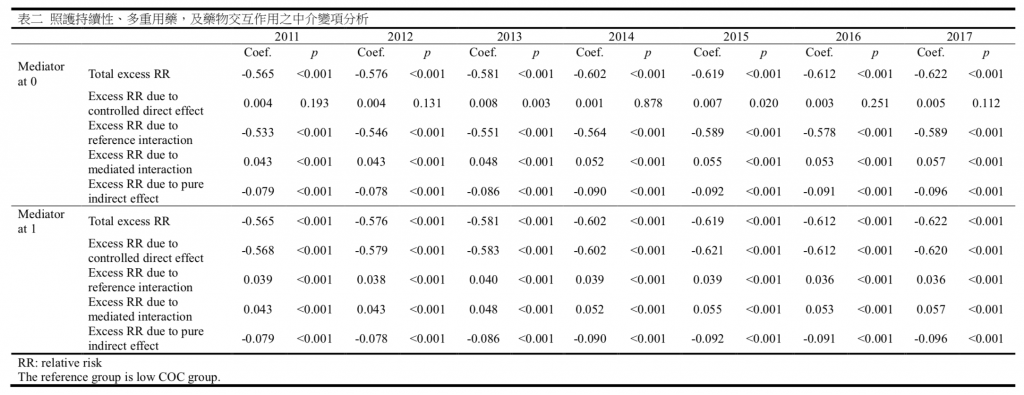
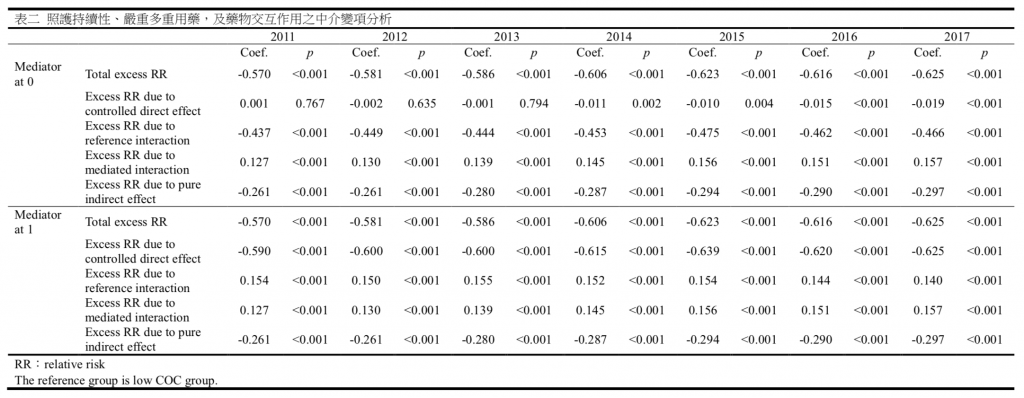
表二和表三呈現了照護持續性,多重用藥或嚴重多重用藥與藥物交互作用之間關係的四向分解結果。表中的估計值表示額外相對風險,顯示照護持續性的效果,以及將總效果拆解後,各組成可以增加或降低的額外相對風險,包括 CDE, INTref,INTmed 和 PIE。其中,CDE 的估計是將中介因子固定在特定水平上進行 的。在表 3 中,以多重用藥為中介因子,2011 年總效果造成的額外相對風險估計為-0.565(p <0.001),高照護持續性組的藥物交互作用事件發生率比低照護持續性組下降了 56.5%。而當我們使用嚴重多重用藥作為中介因子時,發現了相似的結果。在表四中,總效果的額外相對風險為-0.570(p <0.001)。這兩種模型的總效果 在各年都有所下降。照護持續性對藥物交互作用事件的效果中,中介作用的額外相對風險為顯著的;因多重用藥而產生的效果在-0.079 至-0.096 之間(p <0.001), 而因嚴重多重用藥而產生的效果則更大,在-0.261 至-0.297 之間(p <0.001)。而照護持續性與多重用藥狀態的交互作用則會增加藥物交互作用事件的發生。
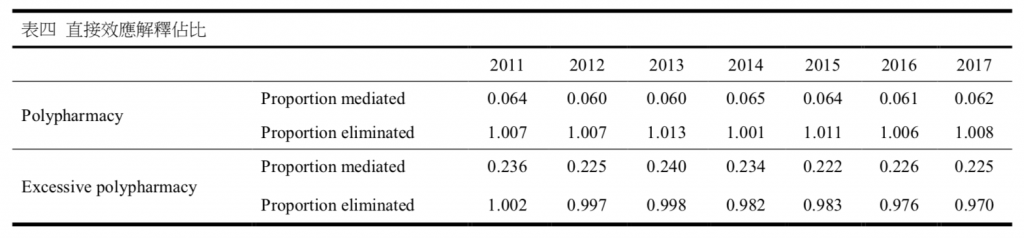
表四呈現中介作用在整體效果中所佔之比例和透過對中介因子的干預後可消除的效果比例,而將中介因子設置在非多重用藥及非嚴重多重用藥的水平上。 40 我們發現,使用嚴重多重用藥作為中介因子比使用多重用藥作為中介因子時,中介作用所占比例更大。而從透過對中介因子的干預後可消除的效果比例顯示, 如果沒有多重用藥,那麼就不會直接受到照護持續性的保護,甚至可能有害。但是控制嚴重多重用藥,仍然可以透過提高照護持續性減少藥物交互作用的發生。 我們按性別和年齡對研究對象進行了分層分析,並比較了兩組之間的效果差異。在對性別的分析中,我們發現在使用嚴重多重用藥作為中介因子的模型中, 中介效果的比例在幅度上更為顯著。在研究期間中介效果的比例沒有太大變化。 另外我們發現,使用不同的中介因子,交互作用的比例(即(INTref + INTmed)/ TE) 存在很大差異。在使用嚴重多重用藥作為中介因子的模型中,約有 50%的效果 是由於交互作用引起的; 但在使用多重用藥作為中介因子的模型中,這一比例 接近 90%。 在兩個模型中,女性的交互作用比例均高於男性。
為了分析年齡的影響,我們將研究人群分為 3 組:65 至 74 歲,75 至 84 歲 和 85 歲以上。研究發現由不同中介因子和年齡組中介作用的比例存在差異。 在以嚴重多重用藥為中介因子的 85 歲以上人群中,中介作用的比例最高,但在以 多重用藥為中介因子的 65 至 74 歲的人群中,中介作用的比例最高。不同年齡組中的交互作用的比例沒有明顯差異。
為了測試結果的可信度,我們按照方法中所述更改了照護持續性和藥物交互作用的定義,進行了敏感性分析,而結果仍然相同。也就是說,較高的照護持續 性與較少的藥物交互作用事件有關,並且這種效果部分地來自多重用藥的中介效果。
我們將多重用藥和嚴重多重用藥重新定義為持續一年的持續狀態,發現過對中介因子的干預後可消除的效果比例和中介效果比例的結果是不同的。所中介效果比例遠低於最初定義的比例,即多重用藥和嚴重多重用藥。持續性嚴重多重用 藥的中介效果比例低於嚴重多重用藥。但持續性多重用藥和多重用藥之間只有微小的差異。
結果討論
在這項研究中我們探討了照護持續性對老年患者藥物交互作用的效果是否會受到多重用藥的中介作用影響。我們的結果建議應透過政策干預多重用藥來發揮照護持續性減少藥物交互作用之效果。我們的研究藉由研究照護持續性的機制影響,並分析其效果組成,提出能可能改善的方向建議,這也是過去研究很少探討之議題。研究結果顯示,老年人經常使用多種藥物,這與以前的研究相似。17,20 台灣的多重用藥情況比其他國家更嚴重。9,41,42 在台灣多重用藥的普遍性可能是由於較高的就醫頻率;我們的研究結果顯示研究對象平均每年有 30 次就診紀錄,而其中約有三分之二的人一年內達 17 次以上。由於台灣缺乏適當的轉診系統,患者可自行選擇醫生而導致照護持續性較低。2 我們發現照護持續性與多重用藥 之間為負相關,因此更好的照護持續性可以防止患者發生多重用藥。另外,多重用藥與藥物交互作用呈正相關,證實多重用藥為藥物交互作用的風險因子。
在中介作用分析中,我們發現增強照護持續性對藥物交互作用事件具有保護作用。但是,在效果拆解後,發現多重用藥和嚴重的多重用藥會發揮不同的效果。 當我們將介入狀態設為沒有多重用藥或沒有嚴重多重用藥時,照護持續性對藥物交互作用事件的影響主要是由於照護持續性和多重用藥狀態之間的交互作用。當多重用藥或嚴重多重用藥時,其保護作用來自照護持續性的直接作用。嚴重多重用藥進行的單純間接效果比多重用藥更大。照護持續性和嚴重多重用藥之間的交互作用大於照護持續性和多重用藥之間的交互作用,因此區分患者的多重用藥狀態至關重要。對於那些被定義為擁有多重用藥(即同時使用 5 種以上藥物)的病患來說,提高其照護持續性可能就已足夠達保護效果,因大部分效果屬於直接效果。但如果為嚴重多重用藥的病人,那麼提高照護持續性可能還不夠。照護持續性和嚴重多重用藥之間的交互作用對藥物交互作用產生負向影響的可能解釋是,由於醫生不了解藥物交互作用的可能反應,他們可能會開出更多用於症狀控制的 藥物。對於嚴重多重用藥患者,要處理其藥物交互作用問題,則需要考慮加上提高照護持續性以外的其他方法。
在次族群分析中,我們選擇性別和年齡作為分組標準,因為不同性別可能有不同的就醫行為。37-39 我們的研究表明,照護持續性對藥物交互作用事件的影響 的組成效果在男性和女性中是不同的。這可能是由於女性比男性更傾向於向醫生諮詢,而高就醫次數造成女性的照護持續性低於男性。女性對藥物治療常持更積 極的態度也可能會有更高的服藥意願。在分析照護持續性對不同年齡組藥物交互作用事件的影響時,在使用嚴重多重用藥作為中介因子的模型中,效果組成有更大差異。85 歲以上的年齡組的對中介因子的干預後可消除的效果比例低於其他年齡組。可以假定這是由於該年齡組的治療可能趨於更保守。12 因此,除了藥物史外,由熟悉情況的固定醫師照顧可能會有所幫助。
控制藥物數量可能是增強照護持續性減少藥物交互作用效果的有效方法。近 期的研究和政策主要側重於減少潛在的不適當藥物(PIM)。許多準則,例如 Beer 準則和 STOPP / START 準則,被開發及用來檢核和評估藥物治療的適當性,達到減少不適當用藥及藥物數量。43,44 但是,即使是符合各項準則所開立的藥物治 療仍可能會給患者帶來其他風險,例如藥物交互作用。為了解決該問題,應當考慮針對藥物交互作用高度相關的多重用藥進行介入處理。過去的研究顯示藥師在減少多重用藥中發擔任要角色。25,45 定期進行藥歷整合及調整藥物有助於減少藥物數量並減輕多重用藥所造成的負擔。為藥物交互作用設置監控計劃則可以確保患者安全。
現今電腦輔助系統已在醫療機構中廣泛採用。 台灣也於 2013 年建立了雲端藥歷系統,將各級醫療院所的健保用藥資料利用雲端分享,成為治療和藥物評估的有力工具。46 但是,目前的利用率和系統滿意度仍待提高。47 儘管該系統可以 提高醫療品質,但一項調查顯示,醫生仍然會抗拒使用此系統。抗拒的原因有許多,而其中一項即為系統操作上仍存在許多不方便之處。48 若能改善資訊提供的品質,則可以有效提升醫療人員使用該項設備的意願。針對多重用藥設置提醒, 則能有效提醒醫療人員評估藥物使用以及發現潛在的藥物交互作用。
本研有些許研究限制,在解讀研究結果時,也必須將這些限制考量在內。首先,因為資料庫的限制,我們只能使用保險資料中所擁有的人口特性資料(如: 性別、年齡),仍有未能被納入的人群特性(如:教育程度)會影響人們的就醫及 用藥行為。42,49 其次,我們透過申報資料,無法得知真正的服藥順從性,也只能確認這些藥物交互作用組合被開立而已。然而,由於本研究所選擇的藥物組合皆為有嚴重臨床後果者,因此這些藥物被開立在病人身上,無論服藥順從性,都是重要的公衛議題。最後,因為醫療體系的不同會影響照護持續性和其效果,我們的研究結果可用於擁有相似的醫療大環境及保險體系國家。35
藥物交互作用和多重用藥都是老年族群中的常見情況,而多重用藥的程度將會影響照護品質。在這項研究中,我們發現多重用藥是照護持續性與藥物交互作用之間關係的部分中介因子,而中介的效果會因多重用藥的程度而異。這項研究提供了實證以支持管理多重用藥之重要性。45 此外,應針對年齡,性別和多重用藥狀況將病患進行特性分類,並制定不同的政策介入。我們的研究為照護持續性的政策提供了精進的方向。
1. Haggerty JL, Reid RJ, Freeman GK, Starfield BH, Adair CE, McKendry R. Continuity of care: a multidisciplinary review. BMJ. 2003;327(7425):1219-1221.
2. Chu H-Y, Chen C-C, Cheng S-H. Continuity of care, potentially inappropriate medication, and health care outcomes among the elderly: evidence from a longitudinal analysis in Taiwan. Medical care. 2012:1002-1009.
3. Chen C-C, Tseng C-H, Cheng S-H. Continuity of care, medication adherence, and health care outcomes among patients with newly diagnosed type 2 diabetes: a longitudinal analysis. Medical care. 2013:231-237.
4. Guo J-Y, Chou Y-J, Pu C. Effect of continuity of care on drug-drug interactions. Medical care. 2017;55(8):744-751.
5. Jazbar J, Locatelli I, Horvat N, Kos M. Clinically relevant potential drug–drug interactions among outpatients: a nationwide database study. Research in Social and Administrative Pharmacy. 2018;14(6):572-580.
6. Obreli-Neto PR, Nobili A, de Oliveira Baldoni A, et al. Adverse drug reactions caused by drug–drug interactions in elderly outpatients: a prospective cohort study. European journal of clinical pharmacology. 2012;68(12):1667-1676.
7. Juurlink DN, Mamdani M, Kopp A, Laupacis A, Redelmeier DA. Drug-drug interactions among elderly patients hospitalized for drug toxicity. Jama. 2003;289(13):1652-1658.
8. Marengoni A, Onder G. Guidelines, polypharmacy, and drug-drug interactions in patients with multimorbidity. In: British Medical Journal Publishing Group; 2015.
9. Slabaugh SL, Maio V, Templin M, Abouzaid S. Prevalence and risk of polypharmacy among the elderly in an outpatient setting. Drugs & aging. 2010;27(12):1019-1028.
10. Cheng S-H, Chen C-C. Effects of continuity of care on medication duplication among the elderly. Medical care. 2014;52(2):149-156.
11. Tsuji-Hayashi Y, Fukuhara S, Green J, Kurokawa K. Use of prescribed drugs among older people in Japan: association with not having a regular physician. Journal of the American Geriatrics Society. 1999;47(12):1425-1429.
12. Lu W-H, Wen Y-W, Chen L-K, Hsiao F-Y. Effect of polypharmacy, potentially inappropriate medications and anticholinergic burden on clinical outcomes: a retrospective cohort study. Canadian Medical Association Journal. 2015;187(4):E130-E137.
13. Smedby Ö, Eklund G, Eriksson EA, Smedby B. Measures of continuity of care: A register-based correlation study. Medical care. 1986:511-518.
14. Pollack CE, Hussey PS, Rudin RS, Fox DS, Lai J, Schneider EC. Measuring care continuity: a comparison of claims-based methods. Medical care. 2016;54(5):e30.
15. Bice TW, Boxerman SB. A quantitative measure of continuity of care. Medical care. 1977;15(4):347- 349.
16. Masnoon N, Shakib S, Kalisch-Ellett L, Caughey GE. What is polypharmacy? A systematic review of definitions. BMC Geriatrics. 2017;17(1):230.
17. Chan D-C, Hao Y-T, Wu S-C. Polypharmacy among disabled taiwanese elderly. Drugs & aging. 2009;26(4):345-354.
18. Dookeeram D, Bidaisee S, Paul JF, et al. Polypharmacy and potential drug–drug interactions in emergency department patients in the Caribbean. International journal of clinical pharmacy. 2017;39(5):1119-1127.
19. Doan J, Zakrzewski-Jakubiak H, Roy J, Turgeon J, Tannenbaum C. Prevalence and risk of potential cytochrome p450–mediated drug-drug interactions in older hospitalized patients with polypharmacy. Annals of Pharmacotherapy. 2013;47(3):324-332.
20. Wang Y-J, Chiang S-C, Lee P-C, et al. Is excessive polypharmacy a transient or persistent phenomenon? A nationwide cohort study in Taiwan. Frontiers in pharmacology. 2018;9:120.
21. Marusic S, Bacic-Vrca V, Neto PRO, Franic M, Erdeljic V, Gojo-Tomic N. Actual drug–drug interactions 8 in elderly patients discharged from internal medicine clinic: a prospective observational study. European journal of clinical pharmacology. 2013;69(9):1717-1724.
22. Nobili A, Pasina L, Tettamanti M, et al. Potentially severe drug interactions in elderly outpatients: results of an observational study of an administrative prescription database. Journal of clinical pharmacy and therapeutics. 2009;34(4):377-386.
23. Johnell K, Klarin I. The Relationship between Number of Drugs and Potential Drug-Drug Interactions in the Elderly. Drug Safety. 2007;30(10):911-918.
24. Malone DC, Armstrong EP, Abarca J, et al. Identification of serious drug–drug interactions: results of the partnership to prevent drug–drug interactions. Journal of the American Pharmacists Association. 2004;44(2):142-151.
25. Cornu P, Steurbaut S, Šoštarić S, Mrhar A, Dupont AG. Performance of a clinical decision support system and of clinical pharmacists in preventing drug–drug interactions on a geriatric ward. International journal of clinical pharmacy. 2014;36(3):519-525.
26. Phansalkar S, Desai AA, Bell D, et al. High-priority drug–drug interactions for use in electronic health records. Journal of the American Medical Informatics Association. 2012;19(5):735-743.
27. McEvoy DS, Sittig DF, Hickman T-T, et al. Variation in high-priority drug-drug interaction alerts across institutions and electronic health records. Journal of the American Medical Informatics Association. 2017;24(2):331-338.
28. Cornu P, Phansalkar S, Seger DL, et al. High-priority and low-priority drug–drug interactions in different international electronic health record systems: A comparative study. International journal of medical informatics. 2018;111:165-171.
29. VanderWeele T. Explanation in causal inference: methods for mediation and interaction. Oxford University Press; 2015.
30. Kline RB. The mediation myth. Basic and Applied Social Psychology. 2015;37(4):202-213.
31. Jiang Z, VanderWeele TJ. When is the difference method conservative for assessing mediation? American journal of epidemiology. 2015;182(2):105-108.
32. Valeri L, VanderWeele TJ. Mediation analysis allowing for exposure–mediator interactions and causal interpretation: theoretical assumptions and implementation with SAS and SPSS macros. Psychological methods. 2013;18(2):137.
33. VanderWeele TJ. A unification of mediation and interaction: a four-way decomposition. Epidemiology (Cambridge, Mass). 2014;25(5):749.
34. Discacciati A, Bellavia A, Lee JJ, Mazumdar M, Valeri L. Med4way: a Stata command to investigate mediating and interactive mechanisms using the four-way effect decomposition. International Journal of Epidemiology. 2018;48(1):15-20.
35. Shin DW, Cho J, Yang HK, et al. Impact of continuity of care on mortality and health care costs: a nationwide cohort study in Korea. The Annals of Family Medicine. 2014;12(6):534-541.
36. Chan DC, Hao YT, Wu SC. Characteristics of outpatient prescriptions for frail Taiwanese elders with long-term care needs. Pharmacoepidemiology and drug safety. 2009;18(4):327-334.
37. Hong JS, Kang HC, Kim J. Continuity of care for elderly patients with diabetes mellitus, hypertension, asthma, and chronic obstructive pulmonary disease in Korea. Journal of Korean medical science. 2010;25(9):1259-1271.
38. Bertakis KD. The influence of gender on the doctor–patient interaction. Patient education and counseling. 2009;76(3):356-360.
39. Hofer-Dückelmann C. Gender and polypharmacotherapy in the elderly: a clinical challenge. In: Sex and Gender Differences in Pharmacology. Springer; 2013:169-182.
40. VanderWeele TJ. Policy-relevant proportions for direct effects. Epidemiology (Cambridge, Mass). 2013;24(1):175.
41. Wastesson JW, Morin L, Laroche ML, Johnell K. How chronic is polypharmacy in old age? A longitudinal nationwide cohort study. Journal of the American Geriatrics Society. 2019;67(3):455- 9 462.
42. Midão L, Giardini A, Menditto E, Kardas P, Costa E. Polypharmacy prevalence among older adults based on the survey of health, ageing and retirement in Europe. Archives of gerontology and geriatrics. 2018;78:213-220.
43. Panel AGSBCUE, Fick DM, Semla TP, et al. American Geriatrics Society 2019 updated AGS Beers Criteria® for potentially inappropriate medication use in older adults. Journal of the American Geriatrics Society. 2019;67(4):674-694.
44. O’Mahony D, O’Sullivan D, Byrne S, O’Connor MN, Ryan C, Gallagher P. STOPP/START criteria for potentially inappropriate prescribing in older people: version 2. Age and ageing. 2015;44(2):213- 218.
45. Chumney EC, Robinson LC. The effects of pharmacist interventions on patients with polypharmacy. Pharmacy Practice. 2006;4(3):103.
46. Huang S-K, Wang P-J, Tseng W-F, et al. NHI-PharmaCloud in Taiwan—A preliminary evaluation using the RE-AIM framework and lessons learned. International journal of medical informatics. 2015;84(10):817-825.
47. Tseng Y-T, Chang EH, Kuo L-N, et al. Preliminary physician and pharmacist survey of the National Health Insurance PharmaCloud system in Taiwan. Computer methods and programs in biomedicine. 2017;149:69-77.
48. Hsieh P-J, Lin W-S. Explaining resistance to system usage in the PharmaCloud: A view of the dualfactor model. Information & Management. 2018;55(1):51-63.
49. Clyne B, Cooper JA, Boland F, Hughes CM, Fahey T, Smith SM. Beliefs about prescribed medication among older patients with polypharmacy: a mixed methods study in primary care. Br J Gen Pract. 2017;67(660):e507-e518. 10
表一 樣本特性(2011)
表二 照護持續性、多重用藥,及藥物交互作用之中介變項分析
表三 照護持續性、嚴重多重用藥,及藥物交互作用之中介變項分析
表四 直接效應解釋佔比